Dépistage du carcinome hépatocellulaire lors d’une maladie chronique du foie
Auteure:
Dre méd. Caroline Bastid
Service de gastro-entérologie et d’hépatologie
Hôpitaux Universitaires de Genève
E-mail: caroline.bastid@hug.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le dépistage du carcinome hépatocellulaire (CHC) permet une détection précoce chez des patients présentant une cirrhose ou des facteurs de risque identifiés dans un contexte de maladie chronique du foie. Les modalités de dépistage peuvent varier en fonction des recommandations spécifiques des différentes sociétés savantes. Elles incluent généralement une échographie abdominale semestrielle pouvant être éventuellement associée à un dosage de alpha-fœtoproteine (AFP).
Keypoints
-
Le CHC représente un enjeu oncologique majeur du 21e siècle nécessitant un dépistage et une prise en charge précoce afin de diminuer la morbi-mortalité associée.
-
Il est important d’identifier les populations à risque de développer un CHC et de les intégrer dans un programme de dépistage périodique.
-
Celui-ci repose sur une échographie abdominale semestrielle selon les recommandations européennes de l’EASL, pouvant être associée à un dosage de l’AFP selon celles de l’AASLD.
-
Le dépistage de CHC doit être systématique chez les patients présentant une hépatopathie chronique avec facteurs de risque selon les recommandations établies. La présence d’importantes comorbidités ou d’une espérance de vie limitée à court terme doivent cependant la pondérer si elles ne permettent pas la réalisation du traitement adéquat.
-
Le contrôle des facteurs étiologiques de la maladie hépatique ne prévient pas toujours l’apparition des CHC.
Le CHC est la néoplasie maligne la plus fréquente du foie (9 cas sur 10). Il survient le plus souvent sur un terrain d’hépatopathie chronique avancée dans plus de 90% des cas.1 Il représente la 6e cause de décès liée au cancer en Suisse et la 3e cause dans le monde. Lorsque la cirrhose est prouvée, on estime l’incidence de survenue de CHC à environ 2 à 4% par an.
Le dépistage et la prise en charge du CHC représente un réel défi mondial avec une incidence future estimée en 2025 de plus d’un million de nouveaux cas par an.2 Selon les recommandations de l’Organisation Mondiale de la Santé (OMS), la mise en place d’un dépistage organisé a pour but de réduire la mortalité et permettre le traitement précoce d’une maladie. Dans le cadre d’une maladie chronique du foie, il repose sur la fréquence importante du CHC en particulier dans les pays industrialisés, l’identification d’une population à risque bien identifiée, l’existence d’un outil de dépistage à travers l’échographie abdominale et la possibilité d’un traitement précoce curatif pour les tumeurs de petite taille.
L’épidémiologie des différentes étiologies à l’origine de la survenue du CHC est variable selon les pays. Les causes virales, telles que l’hépatite virale B (HVB) et hépatite virale C (HVC) sont prédominantes, en particulier en Asie et en Afrique. On observe cependant une tendance à l’augmentation des maladies du foie liée au syndrome métabolique (MASLD, «metabolic dysfunction-associated steatotic liver disease») et à la consommation d’alcool dans les pays industrialisés, Europe et États- Unis.2
Les facteurs de risque d’apparition de CHC sont la présence d’une cirrhose toutes causes confondues, l’infection HBV, la consommation d’alcool, et la présence d’une maladie du foie liée à une dysfonction métabolique MASLD.
L’étude de Yeo et al. parue en 20213 a mis en évidence une réelle lacune de surveillance d’apparition des complications chez des patients atteints d’une cirrhose, en particulier pour le dépistage de CHC. En effet, sur 83000 cirrhotiques suivis de 2007 à 2016, plus de la moitié des patients n’ont eu aucune imagerie à la recherche d’une lésion tumorale sur l’ensemble de leur suivi. Il est donc primordial que le clinicien soit vigilant vis-à-vis des complications, telles que l’apparition d’un CHC dans un contexte de maladie chronique du foie.
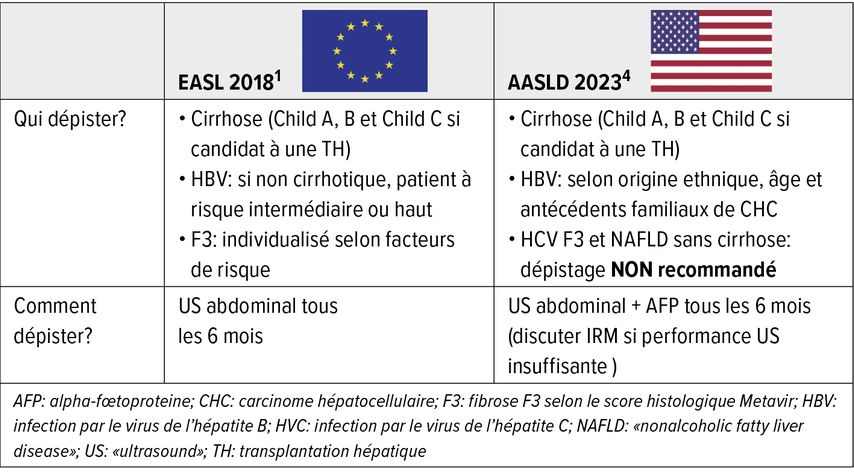
Il existe des différences de recommandations selon les sociétés savantes internationales (Tab. 1). L’ EASL (European Association for the Study of the Liver) a mis à jour les recommandations de dépistage du CHC en 2018.1 L’imagerie de référence est une échographie abdominale à la recherche d’une nouvelle lésion nodulaire du foie qui doit être effectuée tous les 6 mois.
Tab. 1: Recommandations de l’EASL (European Association for the Study of the Liver) et de l’AASLD (American Association for the Study of Liver Diseases) concernant le dépistage du carcinome hépatocellulaire1,4
Elle concerne les patients atteints de cirrhose avec un score de Child Pugh A ou B ainsi que les patients avec un score de Child Pugh C ayant un projet de transplantation hépatique. Les patients atteints d’une HVB chronique sans cirrhose mais associée à un ou plusieurs facteurs de risque sont également concernés. Les personnes présentant une fibrose F3 selon le score histologique Metavir sont également concernés s’il existe des facteurs de risque (voir cas particuliers).
Les recommandations de l’AASLD (American Association for the Study of Liver Diseases) ont été actualisées en 2023.4 Elles préconisent la réalisation d’une échographie abdominale et un dosage de l’AFP tous les 6 mois. L’IRM hépatique est une alternative lorsque l’échographie est peu performante.
La population concernée est constituée également des patients cirrhotiques (score Child Pugh A, B ou C si projet de transplantation hépatique), des patients porteurs d’une HVB chronique avec facteurs de risque identifiés. Le dépistage chez des patients atteints de fibrose F3 selon le score Metavir dans un contexte d’HVC ou de MASLD n’est actuellement pas recommandé.
Cas particuliers
Patients atteints d’hépatite chronique B
Une hépatopathie chronique liée à la présence d’une HVB même en l’absence de fibrose est un terrain favorisant au développement du CHC.5 Les facteurs identifiés favorisant l’apparition de CHC et nécessitant une surveillance semestrielle sont une ethnie d’origine africaine ou asiatique, l’âge, une virémie élevée, la présence d’un antigène HBe, un antécédent de CHC intrafamilial.
La mise en place d’un traitement antiviral semble diminuer le risque d’apparition de CHC après 5 ans de thérapeutique, mais ce risque persiste comme le démontrent Papatheodoridis et al. en 2017.6Dans ce contexte, il est important de continuer de réaliser un dépistage semestriel chez les patients en fonction des facteurs de risque, même lorsqu’un traitement antiviral est présent.
Patients atteints d’hépatite chronique C
La survenue d’un CHC chez les patients atteints d’une HVC chronique est liée à la présence d’une fibrose avancée ou d’une cirrhose. Les avancées scientifiques ont permis une révolution du traitement d’éradication de ce virus avec un succès dans plus de 95% des cas.
Cependant, plusieurs travaux tendent à mettre en alerte quant à la persistance du risque de survenue du CHC. En effet, l’étude d’une cohorte française menée pendant 10 ans sur 174 patients avec fibrose avancée ou cirrhose traitées avec éradication de l’HCV a révélé que 96% des cancers du foie observés sont apparus dans les 5 ans post éradication de l’HCV.7L’éradication d’une HVC ne protège pas de l’apparition de CHC incitant à maintenir un programme de dépistage même lorsque le facteur étiologique est traité.
Patients atteints de MASLD
Un travail réalisé en 2009 par V. Paradis et al. a mis en évidence que plus de la moitié des CHC développés dans un contexte de MASLD survenait sur un terrain en l’absence de fibrose ou dans un contexte de fibrose modérée (F1–F2).8 Selon les constatations de l’AASLD, il représenterait entre 25 et 33% des CHC sur foie non cirrhotiques.4
Les facteurs de risque identifiés sont le mauvais contrôle du diabète, un surpoids ou une obésité, une consommation d’alcool concomitante ainsi qu’un âge avancé. Devant ces différentes données, les recommandations européennes encouragent à mettre en place un dépistage dès le stade de fibrose F3 selon le score Metavir et présence de facteurs de risque même si la balance coût-efficacité est controversée.
Les modalités de dépistage
L’échographie abdominale est un examen facile d’accès, non invasif et non irradiant avec un coût modéré. Il représente l’examen de référence dans le cadre du dépistage du CHC. Certains facteurs peuvent cependant influencer le résultat. Une méta-analyse de 32 travaux publiée en 2018 estime à 84% la sensibilité de l’échographie pour le dépistage de CHC tous stades confondus et d’uniquement 47% pour les lésions à un stade précoce.9 L’exploration de l’ensemble du parenchyme hépatique est parfois plus difficile pour les zones profondes ou au niveau du dôme hépatique. Un terrain de cirrhose sous-jacent avec un aspect nodulaire du foie peut engendrer des faux positifs et diminuer la valeur prédictive positive. Les caractéristiques du patient peuvent limiter l’exploration du foie en cas d’obésité, des gaz intestinaux (jeun non respecté), des antécédents de procédures interventionnelles au niveau hépatique ou encore des particularités anatomiques. La réalisation de cet examen est opérateur dépendant dont l’expertise influencera potentiellement la sensibilité de celui-ci.10–12
Cette détection des lésions tumorales peut être améliorée grâce au recours à l’imagerie en coupe. En particulier, la sensibilité de l’imagerie par résonnance magnétique (IRM) hépatique varie entre 77 à 100%. Celle de la tomodensitométrie (CT) est moindre d’environ 65% tous stades confondus.13,14 La sensibilité est donc meilleure pour l’imagerie en coupe mais représente un coût trop élevé pour son application dans un programme de surveillance actuellement. Il existe d’autant plus des problèmes d’accessibilité, d’allergie aux produits de contraste, de faux positifs et d’irradiation à mettre dans la balance d’un examen qui doit être répété tous les 6 mois. Leur place est actuellement envisagée lorsque l’échographie abdominale est peu performante et en présence de facteurs de risque intermédiaire ou élevé. Des études sont en cours afin d’étudier des alternatives telles que l’IRM à séquence rapide. La fréquence de réalisation reste à définir en raison des facteurs limitants cités ci-dessus. La confirmation de sa place dans un tel programme de dépistage sera évaluée en fonction de son accessibilité et de son coût.
Le dosage de l’AFP est un outil utile validé uniquement dans les recommandations américaines dans le cadre du dépistage du CHC, en association avec une échographie abdominale. Il permettrait une amélioration de la sensibilité de 6 à 8%.15 Il existe des faux positifs en cas d’hépatite active, en particulier virale mais également des faux négatifs dans le cadre de CHC précoce ou de CHC n’exprimant pas l’AFP dans 10 à 20% des cas.16
La fréquence de réalisation des examens de surveillance à effectuer tous les 6 mois est basée sur la vitesse de croissance tumorale jusqu’à sa limite de détectabilité ainsi que sur l’incidence du CHC dans la population cible.17,18
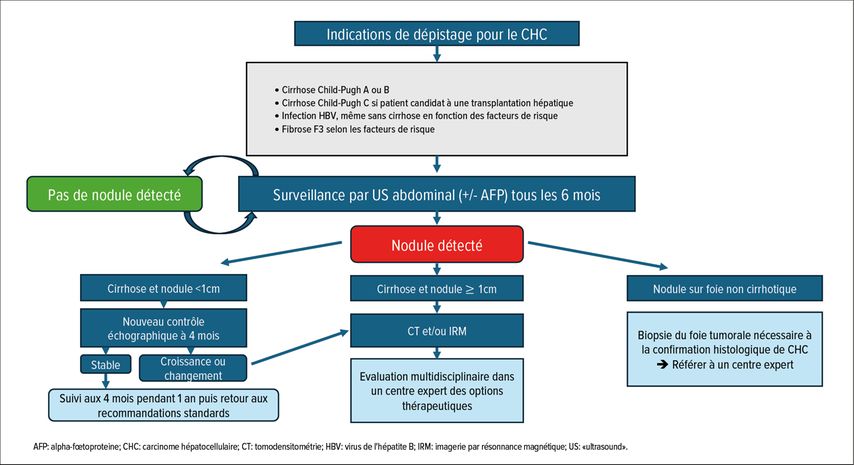
Lors de la découverte d’une lésion suspecte, en fonction de sa taille et du terrain sous-jacent cirrhotique ou non, une imagerie en coupe (IRM hépatique ou CT abdominale 4 phases) est nécessaire afin de mieux la caractériser (Fig. 1). La réalisation d’une biopsie du foie tumorale et non tumorale doit être discutée en réunion multidisciplinaire en centre expert, tel que le Centre des affections hépatobiliaires et pancréatiques des Hôpitaux Universitaires de Genève. Le patient pourra être orienté par la suite vers une équipe spécialisée onco-hépatologique pour la réalisation et le suivi du traitement.
Fig. 1: Recommandations pour le dépistage du carcinome hépatocellulaire adaptées selon les recommandations de l’EASL1,19
La stratégie thérapeutique repose sur les recommandations de la Clinique de Barcelone en fonction de l’état général du patient, de sa fonction hépatocellulaire et des caractéristiques de la tumeur.
Littérature:
1 European Association for the Study of the Liver: EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol 2018; 69: 182-236 2 Llovet JM et al.: Hepatocellular carcinoma. Nat Rev Dis Primer 2021; 7: 6 3 Yeo YH et al.: Surveillance of patients with cirrhosis remains suboptimal in the United States. J Hepatol 2021; 75: 856-64 4 Singal AG et al.: AASLD Practice Guidance on prevention, diagnosis, and treatment of hepatocellular carcinoma. Hepatol 2023; 78: 1922-65 5 Chen CJ et al.: Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. JAMA 2006; 295: 65-73 6 Papatheodoridis GV et al.: The risk of hepatocellular carcinoma decreases after the first 5 years of entecavir or tenofovir in Caucasians with chronic hepatitis B. Hepatol 2017; 66: 1444-53 7 Pascale A: Phenotypic characteristics of primary liver cancer in a large French cohort of patients with viral chronic liver disease followed-up before and after viral eradications: an ANRS study. J Hepatol 2023; 78: S489-9 8 Paradis V et al.: Hepatocellular carcinomas in patients with metabolic syndrome often develop without significant liver fibrosis: a pathological analysis. Hepatol 2009; 49: 851-9 9 Tzartzeva K et al.: Surveillance imaging and alpha fetoprotein for early detection of hepatocellular carcinoma in patients with cirrhosis: A meta-analysis. Gastroenterol 2018; 154: 1706-18 10 Foerster F, Galle PR: Ultrasound for hepatocellular carcinoma surveillance: Still looking for the fortune teller. Liver Transpl 2018; 24: 1167-8 11 Aubry JF et al.: The road to clinical use of high-intensity focused ultrasound for liver cancer: technical and clinical consensus. J Ther Ultrasound 2013; 1: 13 12 Samoylova ML et al.: Predictors of ultrasound failure to detect hepatocellular carcinoma. Liver Transpl 2018; 24: 1171-7 13 Yu NC et al.: CT and MRI improve detection of hepatocellular carcinoma, compared with ultrasound alone, in patients with cirrhosis. Clin Gastroenterol Hepatol 2011; 9: 161-7 14 Burrel M et al.: MRI angiography is superior to helical CT for detection of HCC prior to liver transplantation: an explant correlation. Hepatol 2003; 38: 1034-42 15 Biselli M et al.: A new approach to the use of α-fetoprotein as surveillance test for hepatocellular carcinoma in patients with cirrhosis. Br J Cancer 2015; 112: 69-76 16 Di Bisceglie AM et al.: Serum alpha-fetoprotein levels in patients with advanced hepatitis C: results from the HALT-C Trial. J Hepatol 2005; 43: 434-41 17 Cucchetti A et al.: Estimation of lead-time bias and its impact on the outcome of surveillance for the early diagnosis of hepatocellular carcinoma. J Hepatol 2014; 61: 333-41 18 Trevisani F et al.: Semiannual and annual surveillance of cirrhotic patients for hepatocellular carcinoma: effects on cancer stage and patient survival (Italian experience). Am J Gastroenterol 2002; 97: 734-44 19 Goossens N et al.: Management of hepatocellular carcinoma: SASL expert opinion statement. Swiss Med Wkly 2020; 150: 20296
Das könnte Sie auch interessieren:
Points forts de l’ESC sur l’amylose cardiaque
La simplification de l’algorithme diagnostique, le renforcement de l’attention portée à la maladie et l’énorme augmentation du nombre d’options thérapeutiques ont permis des progrès ...
Le diabète de type 2 peut être prévenu
Une activité physique accrue, un changement des habitudes alimentaires et une perte de poids réduisent le risque de diabète ou peuvent même conduire à une rémission du diabète de type 2 ...
Sarcopénie chez les patient·es atteint·es de cirrhose
La sarcopénie est une maladie musculaire progressive qui s’accompagne d’une perte de masse et de fonction musculaires. Bien qu’environ un tiers des patient·es atteint·es de cirrhose ...