Neue diagnostische Methoden in der Endoskopie und der Funktionsdiagnostik
Autor:
PD Dr.med. Heiko Frühauf
Zentrum für Gastroenterologie und Hepatologie
Zürich
E-Mail: fruehauf@zgh.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der Artikel gibt einen Überblick über eine Auswahl an für Allgemeininternisten relevanten neue(re)n gastroenterologischen Untersuchungsmethoden, die für das klinisch Management von Bedeutung sind. Konkret werden behandelt: Hilfsmittel zur Qualitätsverbesserung bei der Diagnostik und Nachsorge von Kolonpolypen; die neue Klassifikation des ösophagogastralen Übergangs und Befundterminologie nach Fundoplicatio; Klassifikation und Differenzialdiagnose der gastroösophagealen Refluxerkrankung und die Indikation zur Funktionsdiagnostik mittels verschiedener Verfahren zur Langzeit-pH-Metrie und hochauflösender Ösophagusmanometrie; die EndoFLIP®-Impedanzplanimetrie und die esoFLIP®-gesteuerte therapeutische Ballondilatation: eine neue diagnostische Methodik in der Endoskopie; sowie ein Ausblick auf die Atmo®-Kapsel und eine neue Technologie zur allumfassenden Evaluation der pathophysiologischen Mechanismen bei Defäkationsstörungen (Fecobionics®).
Diagnostik und Nachsorge von Kolonpolypen
Verbesserung der Detektion von Kolonpolypen
In vielen Ländern wird die Durchführung einer Screening-Koloskopie zur Suche nach Dickdarmpolypen und damit zur Darmkrebsprävention empfohlen: in der Schweiz bei allen gesunden Personen ab dem 50. Lebensjahr, in Deutschland ab dem 55. Lebensjahr und in den USA ab dem 45. Lebensjahr. Dabei handelt es sich um eine echte Krebsvorsorge im Sinne einer Prävention und nicht nur um eine Früherkennung von Darmkrebs. Da Karzinome entweder auf dem Boden von Adenomen oder sessilen serratierten Läsionen entstehen (sog. Adenom-Karzinom-Sequenz), wird bei der Vorsorgekoloskopie systematisch nach solchen – in der Regel benignen – Polypen gefahndet. Im Gegensatz zu anderen Verfahren der Darmkrebsvorsorge können sie bei dieser Gelegenheit gleich vollständig reseziert werden. Neben der Qualität der Darmvorbereitung, die nach sorgfältiger Aufklärung eine entsprechende Mitarbeit der Patienten erfordert, ist vor allem die Adenomdetektionsrate (ADR) des Arztes für die Qualität einer Vorsorgekoloskopie entscheidend. Eine um 1% höhere Adenomdetektionsrate führt dabei zu einer Reduktion des Auftretens von Intervallkarzinomen von 5%.1
Bereits in den letzten Jahren konnte gezeigt werden, dass für die Inspektion der Mukosa die sogenannte «Rückzugszeit» (d.h., die Zeit, die für die Inspektion der Kolonmukosa aufgewendet wird) dokumentiert werden sollte, um eine möglichst hohe ADR zu erreichen. Diese sollte mindestens 9 Minuten, bei Einsatz der unten genannten technischen Hilfsmittel mindestens 8 Minuten betragen. Eine Verlängerung der Inspektionszeit über diesen Wert hinaus bringt hingegen keinen Vorteil.
Seit einiger Zeit ist auch bekannt, dass die Applikation von N-Butylscopolamin spätestens bei Erreichen des Zökums zu einer Erhöhung der Polypendetektionsrate beiträgt (Anstieg der detektierten Polypen pro Patient von 0,7 auf 0,9).2
In letzter Zeit haben sich zudem Aufsatzkappen für die Endoskope zur Qualitätsverbesserung durchgesetzt. In einer Studie3 konnte gezeigt werden, dass damit mehr Adenome pro Koloskopie detektiert werden. Die auf die Endoskopspitze aufgesetzte Kappe (Endocuff®) besteht aus einem Plastikring mit einem Lamellenkranz, der sich beim Avancieren des Instruments im Kolon dem Endoskop stromlinienförmig anlegt und beim Rückzug aufstellt und die Haustren so zur Seite schiebt und auf diese Weise ermöglicht, auch hinter Falten verborgene Polypen zu erkennen.
Seit einigen Jahren steht zudem eine ergänzend eingesetzte automatisierte Polypendetektion mittels künstliche Intelligenz zur Verfügung. Neben verschiedenen herstellerspezifischen Verfahren wie beispielsweise (EndoAID® von Olympus) oder (CAD EYE® von Fuji) gibt es auch ein plattformübergreifendes System (GI-Genius® von Medtronic), das während der Koloskopie in Echtzeit polypenverdächtige Mukosaläsionen markiert (analog der Gesichtserkennung von Smartphone-Kameras). Im internationalen Sprachgebrauch hat sich die Bezeichnung CADe für «computer aided detection» durchgesetzt. Darüber hinaus sind bereits Prototypen im Einsatz, die auch eine computergestützte Diagnose der detektierten Polypen im Sinne einer Unterscheidung Adenom und Nicht-Adenom, also eine computergestützte Diagnose (CADx – «Computer Aided Diagnosis») ermöglichen (sollen). Ob solche Systeme es zukünftig erlauben, auf die Resektion oder die histopathologische Begutachtung prognostisch irrelevanter Befunde zu verzichten, um Kosten einzusparen, bleibt abzuwarten. Zum gegenwärtigen Zeitpunkt ist dieses Stadium (noch?) nicht erreicht. Dennoch tragen solche KI- und «deep-learning-basierten» Systeme bereits jetzt dazu bei, die Rate «übersehener» Polypen deutlich (ca. um zweifach) zu reduzieren oder 6–10% mehr Polypen zu erkennen.4–6 Für den Anwender undurchsichtig bleibt allerdings, dass nicht genau bekannt ist, in welchen Patientengruppe solche Systeme validiert wurden. Dies ist insbesondere bei solchen KI-Anwendungen zu berücksichtigen, bei denen beispielsweise die ethnische Zugehörigkeit zu einer bestimmten Patientengruppe risiko- oder prognosebestimmend ist.
Neue Nachsorgerichtlinie
Die klinische Relevanz einer gesteigerten Polypendetektionsrate liegt in der korrekten Wahl des Polypennachsorgeintervalls. Diesbezüglich wurden 2022 in der Schweiz von der nationalen Fachgesellschaft neue Nachsorgeempfehlungen publiziert.7 Grundsätzlich wird in dem Schema zwischen adenomatösen Polypen und sessilen serratierten Läsionen unterschieden, da sie sich in ihrer Karzinogenese unterscheiden. Es werden jeweils Situationen mit geringerem von solchen mit hohem Risiko unterschieden (Tab. 1).
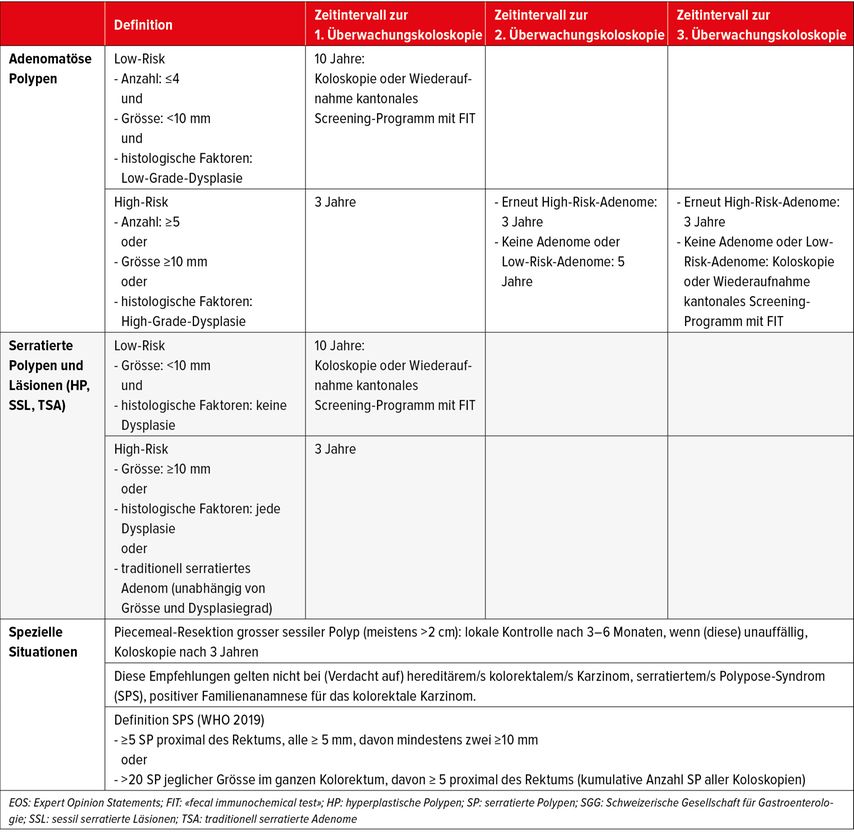
Tab. 1: Konsensus-Empfehlungen zur Nachsorge nach koloskopischer Polypektomie. Voraussetzung: vgl. EOS, SGG-Wegleitung Koloskopie/Screening-Koloskopie (aus Truninger et al.: Swiss Med Forum 2022; 22: 349-55, published under the copyright license CC BY-NC-ND 4.0)7
Bei geringem Risiko (≤4 Adenome jeweils <10mm) wird eine Surveillance-Koloskopie nach 10 Jahren empfohlen, sofern keine höhergradige Dysplasie vorliegt. Bei allen anderen Adenomen wird eine Nachsorgekoloskopie bereits nach 3 Jahren empfohlen. Wenn zu diesem Zeitpunkt eine Situation mit geringem Risiko vorliegt, erfolgt die nächste Surveillance-Koloskopie in 5 Jahren und dann nach dem üblichen Schema. Bei sessilen serratierten Polypen oder Läsionen8 <10mm und ohne Nachweis einer Dysplasie ist ebenfalls erst in 10 Jahren wieder eine Surveillance-Koloskopie zu planen, wohingegen bei höherem Risiko (Polypen von ≥10mm mit jedem Dysplasiegrad oder traditionell serratierten Adenomen unabhängig von Grösse und Dysplasiegrad) eine Surveillance-Koloskopie in 3 Jahren zu empfohlen wird. Die Verlängerung des bisherigen Nachsorgeintervalls von 5 auf 10 Jahre hat unter Ärzten und auch unter den Patienten, die diese Intervalle zum Teil über Jahre gewohnt waren, eine gewisse Unruhe ausgelöst, ist im Hinblick auf ein individualisiertes Vorgehen je nach Risiko aber berechtigt. In dem Zusammenhang ist zu beachten, dass diese allgemeinen Empfehlungen in speziellen Situationen jedoch nicht gelten, beispielsweise nach fraktionierter («piece-meal»-) Resektion grosser sessiler Polypen >2cm, bei positiver Familienanamnese für das kolorektale Karzinom, hereditäre kolorektale Karzinome oder serratierte Polyposissyndrome, definiert als >5 serratierte Polypen proximal des Rektums, alle >5mm, mindestens 2 davon >10mm oder >20 serratierte Läsionen jeglicher Grösse, davon mindestens 5 oberhalb des Rektums (Tab. 1).7
Ösophagogastraler Übergang
Hill-Klassifikation des ösophagogastralen Übergangs
Bei der endoskopischen Diagnostik von Hiatushernien hat sich in den letzten 2 Jahren die sogenannte Hill-Klassifikation durchgesetzt.9 Hierbei wird bei der Gastroskopie in Inversion beurteilt, wie gut die Kardia nach Luftinsufflation das eingeführte Gastroskop umschliesst. Bei engem Kardiaschluss oder allenfalls atmungsabhängiger leichter Öffnung liegt ein Hill-Grad I bzw. II vor, die als Normalbefunde angesehen werden. Bei fehlendem Kardiaschluss um das Gastroskop spricht man von Kadiainsuffizienz, entsprechend einem Hill-Grad III. Wenn in Inversion in eine weit geöffnete Hiatushernie hineingeschaut werden kann, liegt ein Hill-Grad IV vor.
Befundterminologie nach Fundoplicatio
Die endoskopische Beurteilung von Patienten, die eine Fundoplicatio erhalten haben, sollte eine exakte Beschreibung der anatomischen Konfiguration der Lage und Symmetrie der Fundoplicatio-Manschette beinhalten. Üblicherweise findet sich eine semizirkuläre Manschette, die das Endoskop in Inversion umschliesst. Sind Nähte dieser Manschette partiell rupturiert, geht dieser semizirkuläre Aspekt verloren. Bei einer nach intrathorakal dislozierten Fundoplicatio-Manschette entsteht das gastroskopische Bild einer Hiatushernie. Darüberhinaus kann die Manschette verdreht sein («twisted»), erkennbar an einer torquiert in den Fundus hineinziehenden, durch die Manschette bedingten Falte. Ausserdem kann die Manschette nach thorakal «verrutscht» («slipped») sein oder es kann sich neben der Fundoplicatio-Manschette eine paraösophageale Hernie ausbilden. Da derartige anatomische Veränderungen nach Fundoplicatio Beschwerden verursachen können und gegebenenfalls eine Reoperation nach sich ziehen, ist die exakte Befundbeschreibung von grosser Bedeutung.
Gastroösophageale Refluxerkrankung (GERD)
Refluxklassifikation nach der Los-Angeles(LA)-Klassifikation
In den letzten Jahren hat sich die Graduierung einer Refluxösophagitis nach der LA-Klassifikation (Grad A–D) durchgesetzt. Während der Grad A durch mindestens eine Erosion von <5mm Länge am ösophagogastralen Übergang gekennzeichnet ist, müssen bei der Refluxösophagitis LA-Grad B eine oder mehrere Erosionen von >5mm Länge vorliegen. Bei Grad C besteht eine kontinuierliche Verbindung der Erosionen über mindestens zwei Mukosafalten, die aber <75% der Zirkumferenz ausmachen. Bei der Refluxösophagitis LA-Grad D sind mehr als 75% der Zirkumferenz von konfluierenden, fibrinbelegten Ulzerationen betroffen. Die Refluxösophagitis LA-Grad A ist unspezifisch und kann auch bei 5–7% der asymptomatischen Kontrollen beobachtet werden und gilt daher ohne Vorliegen anderer Diagnosekriterien nicht als refluxdefinierende Läsion. Die übrigen LA-Grade sind hingegen refluxdefinierend (speziell Grad C und D) und sollten umgehend Anlass für eine konsequente PPI-Therapie sein. Eine Funktionsiagnostik (pH-Metrie) ist dann für die Diagnosestellung nicht erforderlich.
Zu beachten ist, dass aber nur 30% der therapienaiven Patienten mit Sodbrennen endoskopisch Erosionen aufweisen. Wird die Endoskopie unter einer PPI-Therapie durchgeführt, sinkt die Prävalenz einer erosiven Refluxerkrankung sogar auf <10%. Deshalb wird empfohlen, PPI 2–4 Wochen vor der endoskopischen Diagnostik abzusetzen. Der Nachweis einer intestinalen Metaplasie im Bereich des ösophagogastralen Übergangs, sogenannte Barrettmukosa, gilt ebenfalls als refluxdefinierende Läsion und wird nach der Prag-Klassifikation graduiert. Hierbei beurteilt man die Längenausdehnung der zirkulären Barrettschleimhaut nach kranial, wobei das Ende der Magenfalten den ösophagogastralen Übergang definiert. Darüberhinaus wird die Länge der am weitesten nach kranial reichenden Mukosazunge beschrieben. So bedeutet ein Stadium C3M4 eine zirkuläre Ausdehnung der Barrettmukosa über 3cm mit einer 1cm darüber hinaus nach kranial reichenden Mukosazunge.
Indikationen für eine Langzeit-pH-Metrie
70–90% der Patienten mit Refluxsymptomen haben bei der initialen Endoskopie einen unauffälligen Normalbefund. Dies kann an einer konkomittierenden PPI-Therapie, einer nach PPI-Therapie abgeheilten erosiven GERD liegen oder einer nicht erosiven Refluxerkrankung entsprechen. Differenzialdiagnostisch ist in diesem Fall aber auch an eine Refluxhypersensitivität («hypersensitiver Ösophagus») oder das Vorliegen einer funktionellen Dyspepsie, z.B. vom Typ «epigastrisches Schmerzsyndrom» zu denken. Um dies zu diagnostizieren, sollte eine 24h-Impedanz-pH-Metrie erfolgen. Diese ist auch bei typischen Refluxbeschwerden ohne Besserung auf eine bereits begonnene PPI-Therapie oder bei atypischen oder extraösophagealen, z.B. respiratorischen Beschwerden indiziert und sollte stets vor einer geplanten Antirefluxoperation erfolgen, um den Reflux und die Symptomatik zu quantifizieren und damit die OP-Indikation zu objektivieren. Zur Überprüfung der Diagnose sollte die Untersuchung ohne PPI-Therapie erfolgen, da die Aussagekraft der Methode dann höher ist und mehr Patienten mit einer signifikant positiven Symptomkorrelation identifiziert werden können. Für die Untersuchung wird ein 2–3mm dünner Impedanz-pH-Metrie-Katheter transnasal in den proximalen Magen eingeführt. Neben dem Magen-pH wird über eine weitere pH-Elektrode, die sich 5cm oberhalb des zuvor manometrisch (s.u.) identifizierten unteren Ösophagussphinkters befindet, die Säureexpositionszeit im distalen Ösophagus bestimmt. Impedanzsensoren auf verschiedenen Höhen des tubulären Ösophagus erlauben die Untersuchung des Bolustransports und die Unterscheidung von Schlucken, Luftschlucken oder Refluxepisoden und Luftaufstossen. Dabei ist die Abgrenzung vom sog. «supragastrischen Aufstossen» («supragastric belching») von besonderer Bedeutung. Hierbei handelt es sich um eine Atem-/Verhaltensstörung, bei der Patienten aktiv, aber unbewusst, Luft in den Ösophagus einschlucken und unmittelbar darauf wieder aufstossen, was zu einer Triggerung von sauren Refluxepisoden führen kann. Davon abgegrenzt werden müssen das «Luftschlucken», die Aerophagie, und das Aufstossen von Luft aus dem Magen («gastric belching»).
Die Diagnostik derartiger Krankheitsbilder ist insofern relevant, als diese Patienten in der Regel nicht von einer Antirefluxoperation profitieren und im Gegenteil nach Anlage einer Fundoplicatio-Manschette darüber keine Luft mehr aufstossen können und dann an Blähungen (Luftblase im Magen) leiden. Die Therapie besteht in einer von Logopäden durchgeführten Atemtherapie unter Zuhilfenahme von Techniken der sog. Zwerchfellatmung («diaphragmatic breathing»).
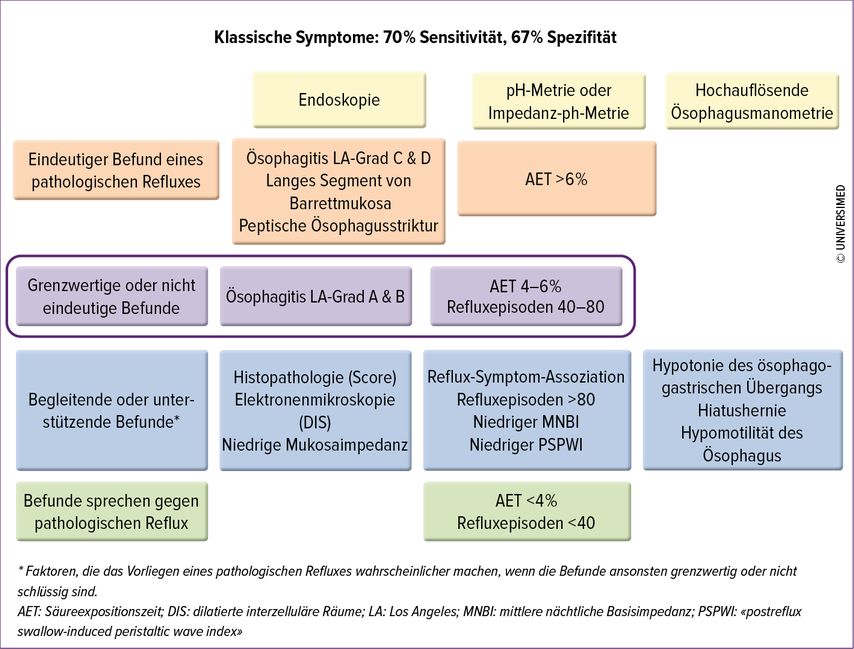
Die Vorteile der 24h-Impedanz-pH Metrie liegen in der Evaluation des Bolustransports im Ösophagus ohne jegliche Exposition gegenüber Röntgenstrahlen und der möglichen Refluxdetektion aller Refluxtyptypen (sauer, nicht sauer, Luft), gegebenenfalls auch unter PPI. Hauptnachteil der Methode ist der häufig als unangenehm empfundene transnasal eingeführte pH-Metrie-Katheter, der die Patienten teilweise in der Wahrnehmung eines üblichen Tagesablaufs doch stärker beeinträchtigt, sodass nicht immer repräsentative Messergebnisse erzielt werden. (Abb. 1)
Abb. 1: Diagnose der gastroösophagealen Refluxerkrankung gemäss Lyon Consensus (nach Gyawali et al., 2018)11
96h-Langzeit-pH-Metrie mittels «drahtloser» BRAVO®-Kapsel
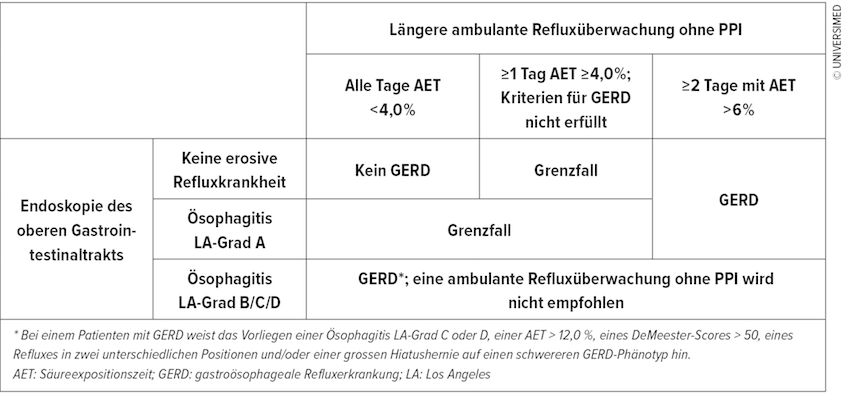
Als alternative Methode zur 24h-Impedanz-pH-Metrie mittels transnasal eingelegtem Katheter hat sich in den letzten Jahren die «drahtlose» 96H-pH-Metrie mit der BRAVO®-Kapsel durchgesetzt. Die Untersuchung ist theoretisch bereits mit der Indexgastroskopie kombinierbar und erlaubt durch das verlängerte Aufzeichnungsintervall die Erkennung einer pathologischen GERD auch bei nur intermittierend auftretendem Reflux. Da die Patienten nicht durch einen transnasalen Katheter beeinträchtigt sind und lediglich das zur Symptomerfassung und pH-Dokumentation erforderliche Aufzeichnungsgerät mitführen müssen gelingt eine repräsentative Messung während des individuellen Tagesablaufs. Die Kapsel wird über ein Applikatorssystem an einer mittels Unterdruck generierten Mukosafalte 6cm oberhalb des ösophagogastralen Übergang (enstprechend 5cm oberhalb des unteren Ösophagussphinkters) mit einer Art Sicherheitsnadel in der Ösophagusmukosa fixiert und fällt nach wenigen Tagen spontan ab. Sie kann ein gewisses Fremdkörpergefühl auslösen, das vor allem für Patienten mit Reflux-Hypersensitivität unangenehm sein kann. Das System kann im Gegensatz zur Impedanz-pH-Metrie allerdings lediglich saure Refluxepisoden detektieren, sodass eine Untersuchung unter PPI nicht sinnvoll ist. Der Einsatz ist bei implantierten Defibrillatoren, Ösophagusvarizen, Divertikeln oder einer Nickel-Kobaltallergie kontraindiziert. Als pathologischer gastroösophagealer Reflux wird bei der BRAVO®-Kapsel-pH-Metrie eine Säureexpositionszeit des distalen Ösophagus von mehr als 6% an mindestens 2 von 4 Tagen gewertet. Ausserdem wird die Symptomkorrelation beurteilt. Die Untersuchung kann helfen, grenzwertige Fälle einer Refluxösophagitis (Endoskopie LA-Grad A) doch einer gastroösopheagealen Refluxerkrankung zuzuordnen (Abb. 2). Studien haben gezeigt, dass eine höhere Anzahl von Tagen mit normaler Säureexposition mit einer 5-fach höheren Wahrscheinlichkeit einhergeht, eine begonnene PPI-Therapie wieder absetzen zu können.
Abb. 2: Indikation zur 48/95h-Langzeit-ph-Metrie mittels drahtloser BRAVO®-Kapsel (nach Yadlapati et al., 2022)12
Hochauflösende Ösophagusmanometrie
Die hochauflösende Ösophagusmanometrie hat bereits seit einigen Jahren einen festen Platz in der Diagnostik von Motilitätsstörungen, der Evaluation des Drucks im unteren Ösophagussphinkter, der Diagnostik von Hiatushernien oder der Funktion einer Fundoplicatio-Manschette, ist aber noch immer nur begrenzt verfügbar. Die Befundung erfolgt mittlerweile anhand standardisierter Diagnosekriterien (aktuell Chicago-4-Klassifikation). Sie erlaubt die Differenzialdiagnose refluxassoziierter oder anderer Motilitätsstörungen bei Dysphagie und sollte stets präoperativ vor geplanten Antirefluxeingriffen erfolgen. Hauptindikation ist der Ausschluss einer Achalasie, da einer von vier Achalasiepatienten über Sodbrennen klagt und sich eine Motilitätsstörung im tubulären Ösophagus als Sodbrennen präsentieren kann. Andererseits hat jeder 10. Patient mit persistierenden Refluxsymptom unter PPI eine Motilitätsstörung, für die eine Antirefluxoperation mit Anlage einer Fundoplicatio-Manschette kontraindiziert sein kann oder bei der Wahl der Operationstechnik Berücksichtigung finden sollte. Differenzialdiagnostisch abgegrenzt werden müssen Patienten mit Ruminationssyndrom. Hierbei kommt es zu einer Regurgitation von Mageninhalt in den Ösophagus aufgrund einer willkürlichen, aber vom Patienten unbewusst erfolgenden kurzen intraabdominellen Druckerhöhung im Moment des Einschluckens, was als «Volumenreflux» fehlinterpretiert werden kann. Etwa jeder 5. Patient mit persistierenden Refluxsymptomen unter einer PPI-Therapie hat ein Ruminationssyndrom, für das eine Antirefluxoperation ebenfalls kontraindiziert ist.
FLIP®: eine neue Methodik in der Endoskopie
Die Bezeichnung «FLIP» ist ein Akronym für «functional lumenal imaging probe». Dabei handelt es sich um einen zylindrischen Ballonkatheter, der während einer Gastroskopie beim sedierten Patienten oral in den Ösophagus bis über den ösophagogastralen Übergang oder mittig im Pylorus platziert wird. Der Ballon wird mit Flüssigkeit gefüllt und das applizierte Volumen und der Druck protokolliert. Über im Ballon vorhandene Impedanzsensoren ist es in Kenntnis dieser Parameter und der gemessenen elektrischen Leitfähigkeit möglich, die Querschnittsfläche (CSA, «cross sectinal area») auf verschiedenen Höhen des Ballons und damit des Ösophagus resp. Pylorus zu ermitteln (daher: «Planimetrie»). Der Quotient aus Querschnittsfläche und Ballondruck wird dabei als «Distensibilitätsindex» (mm2/mmHg) bzw. «Distensibilität» bezeichnet und entspricht klinisch der Dehnbarkeit des ösophagogastralen Übergangs bzw. des Pyloruskanals. Die erhaltenen Messergebnisse werden zudem grafisch über die Zeit aufgetragen. Im angloamerikanischen Sprachraum wird dafür auch der Begriff «Impedanzplanimetrie» verwendet. Es resultiert ein ähnliches farbiges Bild wie bei der hochauflösenden Ösophagusmanometrie («spatio-temporal plot»), wobei hier allerdings nicht die Druckamplituden auf unterschiedlichen Höhen des Ösophagus gegen die Zeit aufgetragen sind, sondern der Durchmesser resp. die Querschnittsfläche. Das Bild reflektiert somit keine direkte Messung der Ösophagusmotilität, sondern die aus dem Distensionsreiz des mit Wasser gefüllten Ballonkatheters resultierenden «sekundären» Kontraktionen anhand der daraus folgenden Änderungen der Querschnittsflächen in vrschiedenen Höhen.
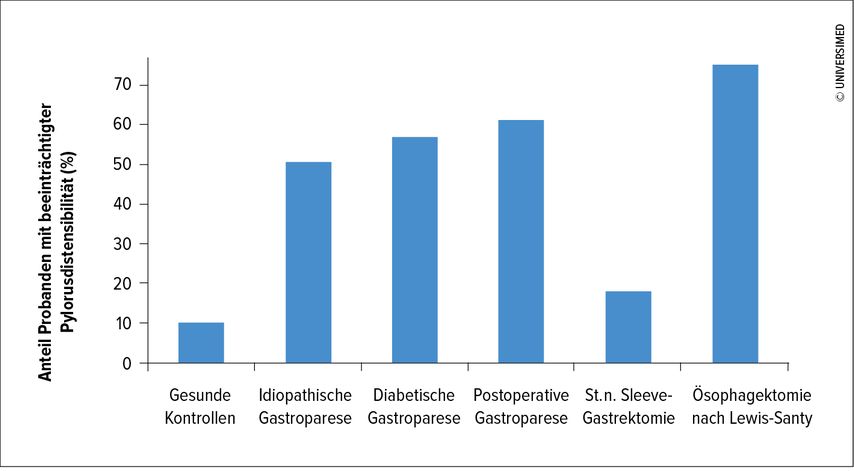
Die EndoFLIP®-Impedanzplanimetrie des ösophagogastralen Übergangs erlaubt den Ausschluss einer Achalasie bzw. den Nachweis einer ösophagogastralen Abflussbehinderung in Sedation während einer Gastroskopie und ist deshalb auch bei Intoleranz von transnasal eingeführten Manometriekathetern eine sehr gute Alternative zur Motilitätsdiagnostik mittels hochauflösender Ösophagusmanometrie. Die Methode kann zudem eine eingeschränkte Pylorusdistensibilität als Hinweis für eine mögliche Magenentleerungsstörung infolge einer funktionellen Magenausgangsstenose oder Pylorusdysfunktion detektieren, die sonst nur mittels Magenentleerungsszintigrafie mit entsprechender Strahlenbelastung oder indirekt über einen 13C-Oktanoat-Atemtest diagnostiziert werden kann. Der Distensibilitätsindex und der Durchmesser des Pyloruskanals ist dabei vor allem bei Patienten mit verzögerter Magenentleerung infolge einer Gastroparese unterschiedlicher Ätiologie und bei Patienten nach Vagusverletzung z.B. nach Ösophagektomie eingeschränkt, weniger ausgeprägt aber auch bei Patienten mit St.n. Schlauchmagen («sleeve»-Gastrektomie) in bariatrischer Indikation vermindert (Abb. 3).
Abb. 3: Beeinträchtigte Pylorusdistensibilität bei verschiedenen Magenpathologien (nach Desprez et al., 2020, und Desprez et al., 2021)13, 14
Bei der diabetischen Gastroparese ist der Pylorusdistensibilitätsindex unabhängig von der Symptomatik und von Diabetesparametern wie dem HbA1c, GLP-1, der diabetischen Retinopathie, Nephropathie oder Neuropathie. Der Vorteil der Methodik liegt insbesondere darin, dass bei nachgewiesener verminderter Distensibilität direkt in der gleichen Sitzung eine als «EsoFLIP®» bezeichnete sog. endoskopischkontrollierte therapeutische Dilatation des Pylorus durchgeführt werden kann (esoFLIP®-gesteuerte therapeutische Ballondilatation). Nach der Therapie, sei es mittels Dilatation, Injektion von Botulinumtoxin oder auch einer peroralen endoskopischen Myotomie (POEM) steigt die Distensibilität typischerweise an.
Ausblick auf zwei neue möglicherweise vielversprechende funktionsdiagnostische Verfahren
Atmo®-Kapsel
Bei der noch nicht weithin verfügbaren Atmo®-Kapsel handelt es sich um einen kapselbasierten Test zur Bestimmung der Transitzeiten, der Diagnostik duodenogastraler Refluxereignisse und einer bakteriellen Fehlbesiedlung des Dünndarms. Die Kapsel verfügt über diverse Gyroskope und Sensoren zur Bestimmung der Wasserstoff- und der Kohlendioxidkonzentration, der Anaerobizität, der Temperatur, der relativen Luftfeuchtigkeit sowie der Stärke des Antennensignals. Mithilfe der Gyroskope kann der Kapselüberschlag bzw. die Orientierung der Kapsel im Darm bestimmt werden. Aufgrund charakteristischer Veränderungen dieser Parameter während der Untersuchung (wie z.B. dem Anstieg der CO2-Konzentration) kann die Magenentleerungszeit nach Kapseleinnahme bestimmt werden. Da es zu einer massiven Zunahme der Anaerobizität nach Übertritt der Kapsel ins Zökum kommt, kann zudem die Dünndarmpassagezeit und die Kolontransitzeit bestimmt werden. Kommt es zu einem Anstieg der Wasserstoffkonzentration, während sich die Kapsel noch im Dünndarm befindet, liegt der Verdacht auf eine bakterielle Fehlbesiedlung des Dünndarms vor. Die bisherigen auf diesem Testprinzip basierenden Wasserstoffatemtests sind diesbezüglich deutlich weniger aussagefähig, da der exakte Zeitpunkt, an dem die applizierte Zuckerlösung das Kolon erreicht, nicht bestimmt werden kann und damit keine sichere Differenzierung zwischen einer beschleunigten orozökalen Transitzeit und einer bakteriellen Fehlbesiedlung des Dünndarms möglich ist.
Die Applikation der Kapsel sollte allerdings nicht unter PPI erfolgen, da dann das Kohlendioxidsignal gestört wird, und die Kapsel ist auch nicht MRI-kompatibel. Für die Diagnostik einer bakteriellen Fehlbesiedlung ist zudem die Anwesenheit von Glukose im Dünndarm erforderlich. Die Sensitivität und Spezifität der Untersuchung liegt gemäss Daten vom nordamerikanischen Gastroenterologiekongress nach Shaw und Holtmann14bei 75 und 91%. Die Messergebnisse korrelieren auch gut mit den Befunden aus Duodenalsaftkulturen.
Fecobionics®
Zur Evaluation der Ursache anorektaler Defäkationsstötungen oder bei Stuhlinkontinenz sind bisher eine Reihe unterschiedlicher, einander ergänzender funktionsdiagnostischer Untersuchungsverfahren erforderlich wie die hochauflösende Analmanometrie zur Bestimmung der Sphikterfunktion, Barostat zur Perzeptionsmessung und Bestimmung der Rektalkapzität, die MRI-Defäkografie zur Evaluation der Anatomie des Beckenbodens und struktureller Defäkationsstörungen sowie der Ballonexpulsionstest zur Prüfung der Evakuation. Zukünftig soll die anorektale Funktionsdiagnostik mit nur einem einzigen, als Fecobionics® bezeichneten System erfolgen können. Dabei handelt es sich um ein ballonummanteltes stäbchenartiges Instrument, das mit zahlreichen, unter anderem gyroskopischen Sensoren und einer miniaturisierten Videokamera versehen ist, mit dem der Defäkationsvorgang umfassend während einer einzigen Untersuchung beschrieben werden können soll und das auch den Ballonexpulsionstest ersetzen soll. Publikationen zur weiteren klinischen Prüfung entsprechender Prototypen werden erwartet.
Literatur:
1 Schottinger JE et al.: Association of physician adenoma detection rates with postcolonoscopy colorectal cancer. JAMA 2022; 327: 2114-22 2 Corte C et al.: Hyoscine butylbromide administered at the cecum increases polyp detection: a randomized double-blind placebo-controlled trial. Endoscopy 2012; 44: 917-22 3 Rex D et al.: High-definition colonoscopy versus Endocuff versus EndoRings versus full-spectrum endoscopy for adenoma detection at colonoscopy: a multicenter randomized trial. Gastrointest Endosc 2018; 88: 335-44 4 Wallace MB et al.: Impact of artificial intelligence on miss rate of colorectal neoplasia. Gastroenterol 2022; 163: 295-304 5 Repici A et al.: Efficacy of real-time computer-aided detection of colorectal neoplasia in a randomized trial. Gastroenterol 2020; 159: 512-20 6 Hassan C et al.: New artificial intelligence system: first validation study versus experienced endoscopists for colorectal polyp detection. Gut 2020; 69: 799-800 7 Truninger K et al.: Nachsorge nach koloskopischer Polypektomie und Therapie des kolorektalen Karzinoms. Swiss Med Forum 2022; 22: 349-55 8 Nagtegaal ID et al.: The 2019 WHO classification of tumours of the digestive system. Histopathology. 2020; 76: 182-8 9 Osman A et al.: Esophagogastric junction morphology on Hill‘s Classification predicts gastroesophageal reflux with good accuracy and consistency. Dig Dis Sci 2021; 66: 151-9 10 Gyawali CP et al.: Modern diagnosis of GERD: the Lyon Consensus. Gut 2018; 67: 1351-62 11 Yadlapati R et al.; CGIT GERD Consensus Conference Participants: AGA clinical practice update on the per-sonalized approach to the evaluation and management of GERD: Expert Review. Clin Gastroenterol Hepa-tol 2022; 20: 984-94.e1 12 Desprez C et al.: Pyloric distensibility measurement after gastric surgery: Which surgeries are associated with pylorospasm? Neurogastroenterol Motil 2020; 32: e13790 13 Desprez C et al.: Assessment of pyloric sphincter distensibility and pressure in patients with diabetic gastroparesis. Neurogastroenterol Motil 2021; 33: e14064 14 Ref. DDW 2023 - bei FG nachfragen?
Das könnte Sie auch interessieren:
Horror im Nachtdienst – Management von ösophagealen Notfällen
Um die Nachtdienste möglichst „horrorfrei“ zu halten, sind regelmäßige „Trockenübungen“, Leitlinienkenntnis und Wissen über endoskopische Hilfsmittel entscheidend. Drei Kasuistiken aus ...
Neuroimmunologische Aspekte bei chronisch-entzündlichen Darmerkrankungen
Psychische Belastungssituationen und chronisch-entzündliche Darmerkrankungen sind untrennbar miteinander verbunden, wobei Ursache und Wirkung oft schwer auseinanderzuhalten sind. Die ...
Fallbeispiel: retrograde cricopharyngeale Dysfunktion (R-CPD)
Ein 24-jähriger männlicher Patient stellte sich mit einer Unfähigkeit zu rülpsen sowie ausgeprägtem Meteorismus und anhaltendem abdominellem Spannungsgefühl vor. Die Symptomatik bestand ...