SARS-CoV-2 und das Immunsystem
Bericht:
Dr. Norbert Hasenöhrl
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Welche Aussagen sind mit welchen Antikörpertests möglich, wie lang halten die Antikörper nach Infektion mit SARS-CoV-2 oder Impfung dagegen und welche Rolle spielt das zelluläre Immunsystem? Antworten auf diese Fragen gaben zwei Topexperten in einem „Giftigen Live-Stream“.
Keypoints
-
Die humorale Immunantwort ist nur ein Teil der Gesamtimmunität gegen SARS-CoV-2.
-
Nach Infektion oder Impfung besteht nach derzeitigem Wissensstand eine Schutzwirkung von circa acht Monaten.
-
Es gibt zum aktuellen Zeitpunkt keinen wissenschaftlich fundierten Cut-off-Wert für den Antikörpertiter, der einem Schutzkorrelat entsprechen würde.
-
Eine Kontrolle des Impferfolgs ist aktuell nur bei unklarer immunologischer Reaktionsfähigkeit (z.B. Immunsuppression) zu empfehlen.
-
Die zelluläre Immunität ist entscheidend für die initiale Viruselimination und damit auch für die Schwere des Krankheitsverlaufs bei Covid-19.
-
Die Dauer der protektiven Immunität nach Infektion mit SARS-CoV-2 hängt von vielen Faktoren wie Schweregrad, Begleiterkrankungen, Alter, genetischen Faktoren etc. ab.
-
Die T-Zell-Immunität (CD4) bleibt nach Infektion lange bestehen.
Angeborene Immunität kommt durch unspezifische Abwehrmechanismen zustande, die einen Erreger bekämpfen und ausschalten können. Davon zu unterscheiden ist die erworbene Immunität, die – als Reaktion auf ein bestimmtes Antigen – durch die Ausbildung spezifischer Antikörper und Immunzellen zustande kommt, z.B. bei einer Infektion oder nach einer Schutzimpfung“, erläuterte Dr. Robert Strassl, Abteilung für Klinische Virologie, Klinisches Institut für Labormedizin, Medizinische Universität Wien.
Die Rolle der Antikörper
Bezüglich der sogenannten humoralen Immunreaktion – der Antikörperbildung durch B-Lymphozyten – ist zwischen einer primären und einer sekundären Immunantwort zu unterscheiden. „Die primäre Immunantwort stellt den Erstkontakt des Immunsystems mit dem Antigen dar. Sie verläuft im Vergleich zur sekundären Immunantwort verzögerter und ist vor allem anfangs noch relativ unspezifisch. Es werden zunächst IgM- und dann auch IgG-Antikörper gebildet. Im Zuge dessen kommt es dann auch zur Bildung von langlebigen Plasmazellen im Knochenmark und von Memory-B-Zellen. Diese können bei neuerlichem Erregerkontakt, im Sinne der sekundären Immunantwort, relativ schnell und effizient hochspezifische neutralisierende IgG-Antikörper sezernieren“, berichtete Strassl. Neutralisierende Antikörper gegen SARS-CoV-2 verhindern die Bindung des Virus an die Zellen, d.h. an den ACE-2-Rezeptor, indem sie das Spike-Protein des Virus blockieren.
„Mit laborbasierten Methoden lassen sich sowohl spezifische Antikörper als auch Antigene von Erregern nachweisen, man spricht von Immunoassays“, fuhr der Experte fort. „Bei SARS-CoV-2 haben wir allerdings das Problem, dass wir noch nicht wissen, ab welchem Antikörpertiter mit einer sicheren Immunität zu rechnen ist.“
Qualitative Antikörpertests auf SARS-CoV-2 sind bereits seit Frühjahr 2020 auf dem Markt, quantitative Tests seit Ende 2020.„Es sind inzwischen sehr viele verschiedene Testsysteme erhältlich und es werden immer mehr“, so Strassl. „Das Problem bestehtdarin, dass diese Tests unterschiedliche Einheiten verwenden und daher nur bedingt vergleichbar sind. Hier ist es wichtig, eine Standardisierung zu schaffen.“ Die WHO hat deshalb Ende 2020 einen internationalen Standard ausgegeben, die sogenannten „binding antibody units“ (BAU).
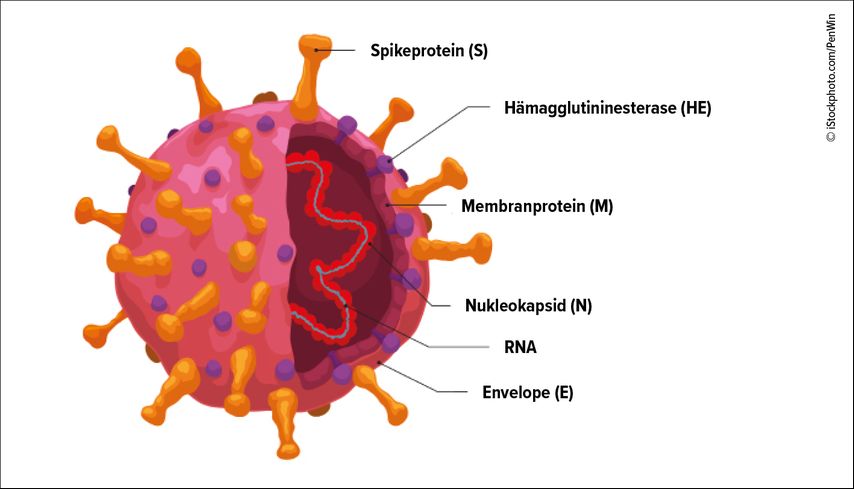
Die meisten Antikörpertests gegen SARS-CoV-2 beziehen sich auf eines von zwei Antigenen: das Spike-Protein (S) oder das Nukleokapsid-Protein (N) (Abb. 1).
N-Antikörper entwickeln sich nur nach einer durchgemachten Infektion, nicht jedoch nach einer Impfung. S-Antikörper hingegen treten sowohl nach Infektion als auch nach Impfung auf – eine Unterscheidung, ob es sich um eine durchgemachte Infektion oder Antikörper handelt, die nach der Impfung ausgebildet wurden, ist anhand der S-Antikörper nicht möglich.
Eine Serokonversion findet im Median zwei Wochen nach Infektion statt (Bereich: 4–22 Tage). Seroprävalenzstudien vom Oktober 2020 haben eine Durchseuchungsrate von ca. 4,7% für Österreich ergeben. „Das bedeutet, dass es, wenn man der Infektion ihren Lauf lässt, bis zum Erreichen einer Herdenimmunität gegen SARS-CoV-2 Jahre dauern würde“, betonte Strassl. „Das unterstreicht die Notwendigkeit der Impfung. Bisherige Studien zeigen, dass die neutralisierenden Antikörper gegen SARS-CoV-2 nach Infektion zumindest zehn bis zwölf Monate nachweisbar bleiben. „Auch langlebige spezifische Plasmazellen waren bis zu elf Monate nach Infektion nachweisbar“, sagte Strassl. Dies führte zur vorläufigen Empfehlung, die Impfung von Genesenen sechs bis acht Monate aufzuschieben, solange Impfstoffknappheit vorlag, und dann zunächst nur eine Impfdosis zu verabreichen. Letzteres beruht auf Studiendaten, die zeigen, dass bei Genesenen die erste Impfung bereits die Funktion einer Boosterung aufweist.
„Da durch die Impfung keine ‚sterilisierende Immunität‘ aufgebaut wird, kann man lediglich sagen, dass jemand, der neutralisierende Antikörper gegen SARS-CoV-2 besitzt, eine geringere epidemiologische Gefahr darstellt als jemand, bei dem das nicht der Fall ist“, betonte der Experte.
Da Neutralisationstests zwar den Goldstandard zum Nachweis einer Schutzwirkung darstellen, aber sehr aufwendig und zeitintensiv sind, greift man auf Surrogatsysteme zurück. „Diese werden meist mit der ELISA-Methode durchgeführt, wobei es aber auch hier durchaus erhebliche Qualitätsunterschiede gibt“, warnte Strassl. „Es gibt aber bei den serologischen Tests eine gewisse Korrelation zum Neutralisationstest.“
Die Kinetik der neutralisierenden Antikörper nach Impfung entspricht im Wesentlichen jener nach durchgemachter Infektion. „Derzeit geht man von einer Schutzwirkung von acht Monaten aus“, erläuterte Strassl. „Eine Impferfolgskontrolle über eine Bestimmung der Antikörpertiter wird bei immunkompetenten Personen derzeit nicht empfohlen“, so der Experte abschließend. „Dies sollte nur bei Personen gemacht werden, bei denen aufgrund ihrer immunologischen Ausgangslage (z.B. immunsupprimierte Patienten) ein geringeres Ansprechen auf die Impfung zu erwarten ist.“
Die Rolle der zellulären Immunität
„Nach dem Eindringen von SARS-CoV-2 in die Zelle wird auf dem Weg über Toll-Like-Rezeptoren eine erste Immunreaktion gestartet, bei der über eine Interferon-Freisetzung unter anderem T-Lymphozyten aktiviert werden“, erklärte Univ.-Prof. Dr. Günter Weiss, Universitätsklinik für Innere Medizin II (Infektiologie, Immunologie, Tropenmedizin, Rheumatologie, Pneumologie), Medizinische Universität Innsbruck.
„Umgekehrt produzieren Coronaviren wie MERS, SARS-CoV-1 und -2 auch Proteine, welche die Signaltransduktion in den befallenen Zellen unterbrechen“, so Weiss. Dies gilt auch für Interferone – die Alpha-Variante von SARS-CoV-2 (B1.1.7,früher: „britische Variante“) scheint ihre höhere Infektiosität dadurch zu gewinnen, dass sie das inhibitorische Protein ORf9b produziert, das die Bildung von Typ-I-Interferonen blockiert. „Die Interferonantwort ist aber ein entscheidender Faktor bei der Kontrolle von Virusinfektionen wie Covid-19“, betonte Weiss.
Am Anfang der SARS-CoV-2-Infektion spielen naturgemäß Zellen der angeborenen Immunität, aber auch bereits CD4-Helferzellen eine Rolle. „Die Qualität der CD4-Immunantwort in dieser Phase ist entscheidend für die Frage, ob es danach zu einer Hyperinflammation und einem Zytokinsturm kommt oder nicht“, erklärte der Experte. Bei schweren Covid-19-Verläufen kann es zu einer Form des sogenannten Makrophagen-Aktivierungssyndroms kommen, wobei sich die massive Ausschüttung von Zytokinen, je nach Ausprägung, nicht nur auf die Lunge, sondern auch auf die Leber und eine ganze Reihe anderer Organe auswirken kann. Die Rolle der CD4-Helferzellen und anderer T-Zell-Subsets beim Zytokinsturm ist noch nicht vollständig geklärt. „Hier scheint es bei Covid-19 eine duale Rolle zu geben – zu wenige CD4-Zellen sind schlecht, aber zu viele ebenfalls“, kommentierte Weiss.
Dysfunktionale Granulo- und Monozyten scheinen als Faktoren für einen schweren Verlauf von Covid-19 eine Rolle zu spielen. „Auch eine Lymphopenie bei Spitalsaufnahme – vor allem der CD4- und CD8-Zellen – ist mit einer schlechten Prognose assoziiert“, ergänzte der Experte. Zudem gibt es eine inverse Korrelation zwischen Lymphozytenzahlen und IL-6-Spiegeln.
„Wir haben also bei schweren Covid-19-Verläufen eine aberrante Immunantwort, die unter anderem durch zu viele neutrophile Granulozyten, zu wenige Lymphozyten und insbesondere auch zu wenige regulatorische T-Zellen gekennzeichnet ist“, fasste Weiss zusammen.
„Nicht vergessen sollte man auch, dass es nicht nur B-Memory-Zellen gibt, sondern auch T-Memory-Zellen, die dafür sorgen, dass bei einem neuerlichen Kontakt mit SARS-CoV-2 die zelluläre Immunität schnell reagieren kann“, so Weiss abschließend.
Quelle:
„Covid-19: Status post bzw. geimpft – was sagen die Antikörper?“, Vortrag im Rahmen des Giftigen Live-Streams vom 10. Juni 2021; verfügbar unter www.infektiologie.co.at/e-learning
Literatur:
bei den Vortragenden
Das könnte Sie auch interessieren:
Lokale Antibiotikatherapie: einige Indikationen mit guter Evidenz
Eine Lokaltherapie mit einem Antibiotikum ist nicht nur an der Haut möglich, sondern kann beispielsweise im Respirationstrakt mittels Inhalation erfolgen. Allerdings besteht bei Weitem ...
Phytotherapie bei Infektionen der Blase und der Atemwege
Heilpflanzen finden seit den frühen Tagen der Menschheit Anwendung bei unterschiedlichsten Erkrankungen. Aktuell besteht das Bemühen, die empirische Anwendung mit Evidenz aus klinischen ...
Hat der Pap-Test in Zeiten der HPV-Impfung noch Zukunft?
Die Inzidenz von Zervixkarzinomen infolge von HPV-Infektionen konnte durch zytologisches Screening in etwa halbiert werden. Mit Einführung der HPV-Impfung besteht nun die Möglichkeit, ...