
Künstliche Intelligenz in der Gastroenterologie und Hepatologie
Autor:
Univ.-Prof. Dr. Peter Fickert
Klinische Abteilung für Gastroenterologie und Hepatologie
Medizinische Universität Graz
E-Mail: peter.fickert@medunigraz.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Digitalisierung der Medizin und zunehmende Anwendung AI(„artificial intelligence“)-assistierter Medizinprodukte in Diagnostik und Therapie gastrointestinaler Erkrankungen schaffen zahlreiche neue Möglichkeiten der Behandlungsverbesserung. Gleichzeitig stehen wir vor großen Herausforderungen. Wir brauchen einen breiten gesellschaftlichen Diskurs, wie wir uns diese neue Medizin vorstellen und wie wir sie haben wollen.
Keypoints
-
Künstliche Intelligenz („artificial intelligence“; AI) ist DER Gamechanger in der Gastroenterologie.
-
Die Endoskopie des Gastrointestinaltrakts wird nach breiter klinischer Einführung eine andere und neue sein.
-
Die Ergebnisse von „deep learning“ werden beinahe alle Bereiche von Diagnostik und Therapie gastrointestinaler Erkrankungen direkt beeinflussen.
-
Die Rolle von uns Ärzt:innen in der Entscheidungsfindung zur Diagnostik und Therapie gastrointestinaler Erkrankungen ist neu zu definieren.
-
Wir müssen JETZT eine Ausbildungsreform einleiten.
Die Dynamik und qualitativen Sprünge aller Formen der Digitalisierung im Bereich der Gastroenterologie und Hepatologie sind atemberaubend. Seit dem Jahr 2020 wurden mehr als 3000 Publikationen zum Thema „artificial intelligence“ (AI) in der Gastroenterologie veröffentlicht. Bereits 2019 fand ein international hochkarätig besetztes Symposium unter dem Titel „First GlobalArtificialIntelligenceinGastroenterologyandEndoscopySummit“ statt, das bereits zum damaligen Zeitpunkt aktuelle (nicht zukünftige!) Anwendungsmöglichkeiten in zahlreichen Gebieten der Gastroenterologie und Hepatologie für AI identifizierte. Als aktuell galten 2019 bereits die Polypendetektion, die Prädiktion der Invasivität von Tumoren im Gastrointestinaltrakt, die Einstufung/Charakterisierung präkanzeröser Läsionen, Kapselendoskopieauswertung, Unterstützung in der Sonografie inklusive des endoskopischen Ultraschalls, Endozytoskopie, verschiedene Anwendungsmöglichkeiten des maschinellen Lernens zur Risikostratifizierung (z.B. bei Leberresektionen, Lebertransplantationen, transarteriellen Chemoembolisationen sowie prädiktive Analysen zur bestmöglichen Therapie bei chronisch-entzündlichen Darmerkrankungen) bis hin zur Verwendung digitaler Symptomtagebücher für Patient:innen.
Der rechtliche Status von Medizinprodukten mit AI
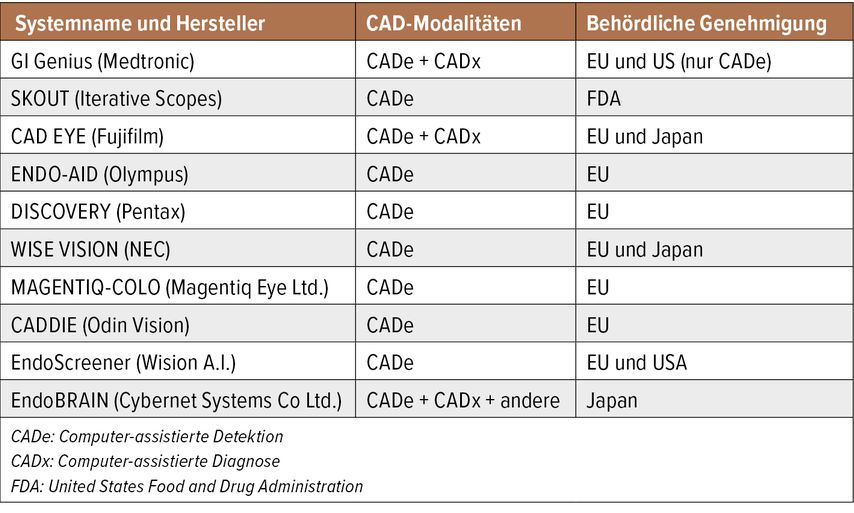
Auch über genaue Klassifikationen für AI-basierte Applikationen und Anwendungen im Bereich der Gastroenterologie und Hepatologie wird seit Beginn der 20er-Jahre unseres Jahrtausends intensiv nachgedacht. Eine solche genaue Klassifizierung (z.B. in Form der Unterscheidung von Software in einem medizinischen Gerät undSoftware als medizinisches Gerät) ist für die Festlegung des rechtlichen Status solcher Medizinprodukte von entscheidender Bedeutung. Erst eine solche Unterscheidung macht eine genaue Kategorisierung von zur Verfügung stehenden oder sich in Entwicklung befindenden Software- oder AI-Produkten möglich, welche aus juridischer Sicht notwendig scheint. Aktuell haben diese Charakterisierungen und erfolgreichen klinischen Erprobungen zur Zulassung zahlreicher computerunterstützter Diagnosegeräte insbesondere auch im Bereich der gastrointestinalen Endoskopie innerhalb der EU geführt. Aktuell steht daher vielerorts in Europa bereits AI als „machine learning software as medical devices“ zur Klassifizierung der Schwere der Kolitis bei chronisch-entzündlichen Darmerkrankungen, zur Detektion von gastrointestinalen Blutungen, zur Detektion von Dysplasien sowie zur Detektion und Klassifizierung von Polypen inklusive einer entsprechenden Therapieempfehlung zur Verfügung. Die entsprechenden Produkte sind in der Tabelle 1 zusammengefasst.
Tab. 1: Computerunterstützte Systeme im Bereich der gastrointestinalen Endoskopie (modifiziert nach Chawla S et al.: Am J Gastroenterol 2021; 116[11]: 2159-62)
Letztendlich für beinahe alle medizinischen Anwendungen AI-assistierter Bildanalysen sind die Begriffe CADe („computer-aided detection“) und CADx („computer-aided diagnosis“) zu unterscheiden. Beispielhaft wäre hier als CADe das alleinige Erkennen von Polypen oder polypenartigen Läsionen bei einer Koloskopie zu erwähnen, wohingegen eine Zuordnung dieser Polypen z.B. nach der NICE-Klassifikation entsprechend Typ I bis Typ III einer CADx entsprechen würde.
Hohe Sensitivitäten und Spezifitäten konnten in der Zwischenzeit in einer Vielzahl hochqualitativer retrospektiver Analysen, aber auch in randomisiert kontrollierten Studien gezeigt werden. Demzufolge liegen Sensitivität und Spezifität bezüglich der Differenzierung von Adenomen und hyperplastisch diminutiven kolorektalen Polypen mittlerweile deutlich über 90%, ebenso wie die Genauigkeit dieser Methoden deutlich über 90% rangiert. Die Ergebnisse dieser Studien wurden relativ rezent in einer Übersichtsarbeit dargestellt (Okagawa Y et al.: Dig Dis Sci 2022; 67(5): 1553-72). Eine vergleichbare Datenfülle wie für die Erkennung und Differenzierung kolorektaler Polypen durch AI-unterstützte Diagnoseverfahren liegt auch zur Detektion und Einstufung von Adenokarzinomen des Ösophagus, Plattenepithelkarzinomen des Ösophagus, Erkennung von Magenfrühkarzinomen sowie zur Klassifizierung chronisch-entzündlicher Darmerkrankungen vor. Insbesondere riesige Datenmengen aus Hochendemiegebieten wie z.B. aus China führten zu einer rasanten Verbesserung der Genauigkeit von Vorsorgegastroskopien beim Magenfrühkarzinom.
Brauchen wir AI in der gastrointestinalen Endoskopie?
Zahlreiche Arbeiten zeigen, dass z.B. im Bereich der Vorsorgekoloskopie eine signifikante Sensitivitäts- und Spezifitätssteigerung und letztendlich damit Qualitätssicherung und Qualitätssteigerung möglich sind. Zudem führt die zusätzliche Verwendung von „Speedometern“, die aktiv die Rückzugszeit bzw. regionalen Verweildauern während des Geräterückzugs erfassen, zu einer weiteren Sensitivitätssteigerung der Untersuchungen. Auch wurde in mehreren, auch kontrollierten Studien gezeigt, dass die Verwendung von AI eine signifikante Verbesserung von Ausbildung und Training in der Endoskopie ermöglicht. Die Verwendung von digitalen Sehschulen/Videorätseln und AI-unterstützter Endoskopie führt zu einer schnelleren Sensibilisierung der Auszubildenden und ermöglicht die Kontrolle und den Abgleich erfasster Bilder bzw. gestellter Diagnosen. Erstaunlicherweise lernen nicht nur Beginne-r:innen in der Endoskopie durch Verwendung von AI-unterstützten Methoden schneller, auch erfahrene nicht AI-trainierte Untersucher:innen können ihre Untersucher:innenqualitäten durch Training mit AI-gestützten Verfahren signifikant verbessern. Letztendlich können durch Verwendung von AI in der Endoskopie bei gezieltem Einsatz und geschulter Verwendung Zeit und Kosten eingespart werden. Beispielhaft sei hier die Vermeidung unnötiger Biopsien oder Polypektomien (z.B. bei hyperplastischen Rektumpolypen) angeführt.
Die größten Herausforderungen
Diese Dynamik in der Entwicklung und Einführung AI-basierter Produkte im Bereich der gastrointestinalen Endoskopie (aber nicht nur dort) stellt die Anwende-r:innen und auch die Krankenanstaltenträger vor enorme strukturelle, personaltechnische und finanzielle Herausforderungen. Neben den Anschaffungskosten sind hier die Notwendigkeit großer Bildspeicher, standardisierter Befundungen und regelmäßiger Software-Updates wohl nur einige der zu nennenden Herausforderungen und Kostentreiber. Niemals sollte man in Personalplanungsmodellen die zur Ausbildung und zum Training nötige Arbeitszeit vergessen! Auch sollte nicht vergessen werden, dass wir in vielen Endoskopien mit völlig veralteten Soft- und Hardwaretechnologien arbeiten (müssen), die länger als 25 Jahre in Verwendung sind – Stichwort: „Endoskopieprogramme“. Eine Entwicklung, die z.B. für die Mobiltelefonie völlig unvorstellbar wäre! Die Gründe dafür sind mannigfaltig, sie sind aber vor allem im hohen Kostenaufwand für die Strukturverantwortlichen (wie Krankenanstaltenträger und Ordinationsinhaber:innen), aber auch im fehlenden Interesse seitens der Industrie zu suchen. Vorstellbar ist auch, dass steigender Wartungsbedarf und zunehmende Haftungsfragen Treiber einer solchen (Nicht-)Entwicklung sind.
Was gibt es sonst noch?
Nicht nur im Bereich bildgebender Verfahren wie der Endoskopie, dem endoskopischen Ultraschall oder der transabdominellen Sonografie stellen Computer-assistierte Diagnoseverfahren einen Paradigmenwechsel in unserem Fach dar. Die personalisierte Medizin im Sinne der Analyse strukturierter und unstrukturierter klinischer Daten wie Labordaten und anamnestischer Angaben sowie die Datenannotierung und darauf folgende Entwicklung von Trainingsmodellen und AI-unterstützten Modellentwicklungen werden für alle Bereiche komplexer gastroenterologischer Erkrankungen wie z.B. chronisch-entzündliche Darmerkrankungen oder das Management fortgeschrittener Lebererkrankungen mit hohem Druck erforscht. Nur durch die Verwendung von AI ist die hochkomplexe Integration von Daten aus bildgebenden Verfahren wie Ultraschall, CT oder MRI zusammen mit histologischen Daten und Biomarkern im Sinne von Entwicklung und Training von AI-gestützten Modellen möglich. So wurden in den letzten vier Jahren zahlreiche Publikationen zur Vorhersage des Wiederkehrens eines hepatozellulären Karzinoms nach Resektion oder nach Lebertransplantation wie auch zum Ansprechen nach transarterieller Chemoembolisation veröffentlicht. Solche Datensätze werden rasch zur Änderung unserer aktuellen Therapiealgorithmen führen. Vergleichbare Analysen und Vorgangsweisen wurden z.B. auch zur Einordnung von Pankreastumoren oder Pankreaszysten entwickelt und erprobt sowie hochkarätig publiziert. Die rasante Entwicklung AI-gestützter Diagnose- und Therapiepfade lässt uns mitunter staunend zurück.
Wann „kommt“ das alles?
Zahlreiche Anwendungsmöglichkeiten von AI-basierten Systemen in der Diagnostik und Therapie gastrointestinaler und hepatologischer Erkrankungen sind nicht Zukunft, sondern bereits Gegenwart. Durch die breite Einführung von AI-basierten Methoden wird in der Gastroenterologie nichts bleiben, wie es ist. Die gastrointestinale Endoskopie wird präziser, schneller und technisch geführter werden, möglicherweise vergleichbar mit der Situation von mit Autopilot fliegenden Flugzeugpilot:innen.
Die Verwendung AI-basierter endoskopischer Methoden wird Standard im Rahmen von klinischen Studien und zunehmend von Patient:innen eingefordert werden und uns vor große strukturelle und finanzielle Herausforderungen stellen. Sehr große zu bewältigende Datenmengen sowie regelmäßig notwendige Updates und Training der Mitarbeiter:innen seien hier erwähnt.
Es wird spannend zu beobachten sein, zu welchem Zeitpunkt in einer S3-Leitlinie erstmals die Verwendung eines spezifischen Algorithmus oder einer AI-basierten endoskopischen Methode gefordert werden wird. Unsere ärztliche Rolle in der Entscheidungsfindung bei Diagnostik und Therapie für gastroenterologische und hepatologische Erkrankungen ist neu zu definieren. Auf diese Herausforderung müssen wir auch ausbildungstechnisch rasch reagieren und adäquate Antworten finden.
Was wäre noch zu bedenken?
-
Bei allen Entwicklungen und Bemühungen müssen unsere Patient:innen im Mittelpunkt bleiben.
-
Zeitgewinn für unsere Patient:innenkontakte bleibt eine zentrale Forderung an die Digitalisierung der Medizin.
-
Die Zielsetzungen von AI-basierten Methoden dürfen nicht primär Zielsetzungen der Medizinökonomie folgen, sondern dem Patient:innenwohl.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Gesundheitskompetenz in der Gastroenterologie und Hepatologie
Die Gesundheitskompetenz hat einen großen Einfluss auf das Gesundheitsverhalten von Patient:innen. Bislang ist allerdings nur wenig hinsichtlich des Wissens der österreichischen ...
Wenn die Magensonde nicht fördert: der seltene Fall eines Magenabszesses
Der vorliegende Fallbericht soll die Aufmerksamkeit auf die seltene Pathologie des Magenwandabszesses lenken, die mit einem eindrucksvollen Ausprägungsgrad initial eine falsche ...
Perioperative Ernährung bei gastrointestinalen Eingriffen
Im Bereich der perioperativen Ernährung bei geplanten Operationen am Magen-Darm-Trakt wurden in den letzten Jahren einige Dogmen über Bord geworfen – mit dem Ziel, den Patienten ...

_A.jpg)
